Te explicamos qué es un cambio químico y cuáles son sus características. Además, ejemplos y diferencias con un cambio físico.

¿Qué es un cambio químico?
Los cambios químicos son un tipo de alteración en la materia que modifica su constitución química, o sea, que altera su naturaleza y no solamente su forma. Esto quiere decir que los cambios químicos, también llamados reacciones químicas o fenómenos químicos, implican ruptura y formación de los enlaces químicos de sustancias o compuestos químicos para formar nuevas sustancias o compuestos.
Las reacciones químicas ocurren cuando se combinan químicamente dos o más sustancias (llamadas reactivos o reactantes) que cambian su estructura química en el proceso, y pueden consumir (reacciones endotérmicas) o liberar (reacciones exotérmicas) energía, para generar dos o más sustancias nuevas (llamadas productos). Algunas reacciones químicas son peligrosas para el ser humano, pues pueden involucrar o producir compuestos tóxicos o corrosivos. Otras reacciones, como es el caso de ciertas reacciones exotérmicas, pueden provocar explosiones.
En la industria química se producen muchos materiales que usamos en la vida diaria mediante reacciones químicas controladas. Algunas reacciones ocurren de forma espontánea y otras deben ser generadas por el ser humano en plantas industriales o en laboratorios químicos.
Las reacciones químicas requieren de un tiempo estipulado para suceder, que varía dependiendo de la naturaleza de los reactivos y de las condiciones en las que la reacción se produzca.
Así, los factores que afectan la velocidad de las reacciones químicas por lo general suelen ser:
- Aumento de temperatura. El aumento de temperatura tiende a aumentar la velocidad de las reacciones químicas.
- Aumento de la presión. Al aumentar la presión se suele aumentar la velocidad de las reacciones químicas. Esto ocurre generalmente cuando reaccionan sustancias que son sensibles a los cambios de presión, como son los gases. En el caso de líquidos y sólidos, los cambios de presión no provocan cambios importantes en la velocidad de sus reacciones.
- Estado de agregación en que se encuentren los reactivos. Los sólidos suelen reaccionar más lentamente que los líquidos o los gases, aunque la velocidad también dependerá de la reactividad de cada sustancia.
- Empleo de catalizadores. Son sustancias que se emplean para aumentar la velocidad de las reacciones químicas. Estas sustancias no intervienen en las reacciones, solo controlan la velocidad a la que ocurren. También existen sustancias llamadas inhibidores, que se emplean de la misma forma pero provocan el efecto contrario, es decir, disminuyen la velocidad de las reacciones.
- Energía luminosa (Luz). Algunas reacciones químicas son aceleradas cuando se les hace incidir luz.
- Concentración de los reactivos. La mayoría de las reacciones químicas ocurre más rápido si tienen una alta concentración de sus reactivos.
Ver también: Producto en química
Ejemplos de cambio químico

Cualquier reacción química es un ejemplo perfecto de cambio químico, incluso las que se dan en nuestros cuerpos. Algunos ejemplos son:
- La respiración. Es un proceso biológico de cambio químico, en el que se toma oxígeno del aire y se lo emplea para reaccionar con la glucosa que obtenemos de los alimentos, generando altos niveles de energía química (ATP) y cantidades de dióxido de carbono (CO2) de desecho, que deben ser expulsadas del organismo.

- La lluvia ácida. Se produce en entornos en los que la atmósfera está muy contaminada. Suele ser el resultado de cambios químicos que se dan entre el agua almacenada en las nubes y otros gases dispersos en el aire, cuyo contenido de óxido de azufre o de óxido de nitrógeno genera ácido sulfúrico o ácido nítrico que caen junto con la lluvia.

- La formación de sales. La reacción que ocurre en el interior de las baterías es producida entre un ácido y un metal. Por ejemplo, en las baterías que utilizan plomo y ácido sulfúrico se produce sulfato de plomo (II), una sal de color blanco.

- La descomposición del ozono. La molécula de ozono se descompone en moléculas de oxígeno por la acción de determinado tipo de luz.

Cambio químico y cambio físico

Los cambios físicos de la materia no alteran su composición, es decir, no modifican la estructura química de las sustancias, por lo que mediante un cambio físico no pueden descomponerse ni formarse sustancias. Los cambios físicos solo cambian propiedades físicas de las sustancias como por ejemplo, la forma, la densidad y los estados de agregación (sólido, líquido, gaseoso). Por otro lado, los cambios físicos suelen ser reversibles, ya que alteran la forma o el estado de la materia, pero no su composición.
Por ejemplo, al hervir agua podremos convertir un líquido en un gas, pero el vapor resultante sigue compuesto por moléculas de agua. Por el contrario, si congelamos el agua, esta pasa al estado sólido, pero igualmente sigue siendo químicamente la misma sustancia. Otro ejemplo es el gas licuado que usamos en nuestros encendedores, que suele ser butano (C4H10) o propano (C3H8) transformados al estado líquido por aplicación de altas presiones, pero sin alterar su composición química.
Los cambios químicos alteran la distribución y los enlaces de los átomos de la materia, logrando que se combinen de manera distinta obteniéndose así sustancias diferentes a las iniciales. Cuando ocurre un cambio químico, siempre se obtiene la misma cantidad de materia que se tenía en un inicio, aunque sea en diferentes proporciones, pues la materia no puede crearse ni destruirse, solo transformarse.
Por ejemplo, si hacemos reaccionar agua (H2O) y potasio (K), obtendremos dos sustancias nuevas: hidróxido de potasio (KOH) e hidrógeno (H2). Esta es una reacción que normalmente libera mucha energía, por tanto, es muy peligrosa.
Sigue con:
Referencias
- “¿Qué es un cambio químico?” https://www.tplaboratorioquimico.com/
- “¿Qué son los cambios químicos?” http://recursostic.educacion.es/
- “Physical and Chemical Changes” (video) en MooMooMath. https://www.youtube.com/
- “Physical and Chemical Changes: Chemistry for Kids” (video) en Free School. https://www.youtube.com/
- “Chemical Change Definition in Chemistry” https://www.thoughtco.com/
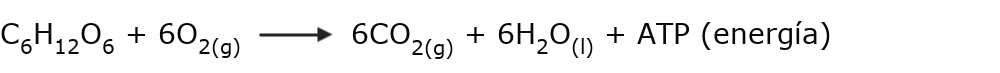
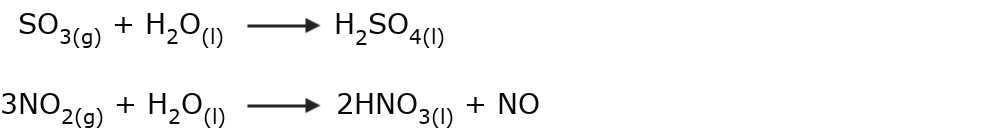
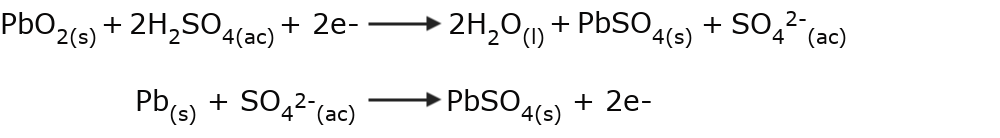





¿Te fue útil esta información?
Sí No¡Genial! Gracias por visitarnos :)