Te explicamos qué es una fórmula química, los tipos que existen, ejemplos y sus partes. Además, los símbolos y elementos químicos.

¿Qué es una fórmula química?
Una fórmula química es una expresión gráfica de los elementos que componen un compuesto químico cualquiera. Las fórmulas expresan los números y las proporciones de sus átomos respectivos y, en muchos casos, también el tipo de enlaces químicos que los unen. A cada molécula y/o compuesto conocido le corresponde una fórmula química, así como un nombre a partir de ella de acuerdo a las reglas de la nomenclatura química.
Existen diversos tipos de fórmulas químicas, cada uno enfocado en cierto tipo de información, pero en líneas generales todas sirven para comprender la naturaleza química de las sustancias y para expresar lo que ocurre durante una reacción química determinada, en la que algunos elementos o compuestos se transforman en otros. Por esa razón, las fórmulas químicas responden a un sistema convencional de representación de los elementos y las moléculas, es decir, a un lenguaje técnico especializado.
Las fórmulas químicas utilizan los símbolos químicos de los elementos y proporciones lógicas entre ellos, expresados mediante símbolos matemáticos.
Ver además: Compuesto inorgánico
Tipos de fórmula química

Existen distintos tipos de fórmula química, útiles para brindar distinta información.
- Fórmula molecular. Es un tipo de fórmula bastante básica que expresa el tipo de átomos presentes en un compuesto covalente y la cantidad de cada uno. Utiliza una secuencia lineal de símbolos de los elementos químicos y números (como subíndices). Por ejemplo, la fórmula molecular de la glucosa es C6H12O6 (seis átomos de carbono, doce de hidrógeno y seis de oxígeno).
- Fórmula semidesarrollada. Similar a la fórmula molecular, es un tipo de fórmula que expresa los átomos que integran el compuesto y expresa también los enlaces químicos (líneas) y su tipo (simples, dobles, triples) entre cada átomo del compuesto. En esta fórmula no se representan los enlaces carbono-hidrógeno. Esto es útil para identificar los grupos radicales que lo conforman, así como su estructura química. Por ejemplo, la fórmula semidesarrollada de la glucosa es, CH2OH – CHOH – CHOH – CHOH – CHOH – CHO .
- Fórmula desarrollada. La fórmula desarrollada es el paso siguiente en complejidad de la semidesarrollada. En esta representación se indica el enlace y la ubicación de cada átomo del compuesto dentro de sus respectivas moléculas, en un plano cartesiano, representando la totalidad de la estructura del compuesto.
- Fórmula estructural. Para representar las moléculas ya no solo en su estructura y organización sino además en su forma espacial, hace falta una fórmula todavía más compleja, que emplea perspectivas bi o tridimensionales.
- Fórmula de Lewis. También llamadas “diagramas de Lewis” o “estructuras de Lewis”, se trata de una representación similar a la fórmula desarrollada de un compuesto, pero que indica los respectivos electrones compartidos en cada enlace químico entre átomos, de acuerdo a la valencia de los elementos involucrados. Estos electrones se representan mediante puntos enlazados con una línea donde hay un enlace. También se representan los electrones no compartidos usando puntos sobre el átomo correspondiente. Son fórmulas muy específicas y de uso técnico.
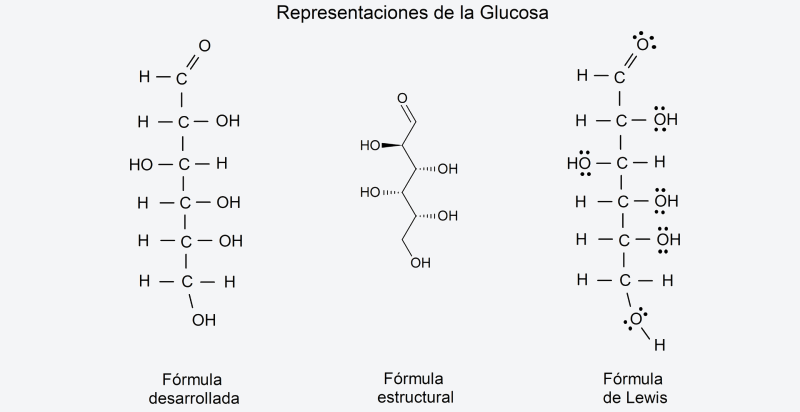
Ejemplos de fórmula química
Algunos ejemplos de fórmula química (molecular) de compuestos conocidos son:
- Oxígeno. O2
- Ozono. O3
- Dióxido de carbono. CO2
- Monóxido de carbono. CO
- Agua. H2O
- Amoníaco. NH3
- Metano. CH4
- Propano. C3H8
- Ácido sulfúrico. H2SO4
- Ácido clorhídrico. HCl
- Cloruro de sodio. NaCl
- Bicarbonato de sodio. NaHCO3
- Formaldehído. CH2O
- Benceno. C6H6
- Sacarosa. C12H22O11
- Cal. CaO
- Alcohol etílico. C2H5OH
- Glutamato monosódico. C5H8NNaO4
- Penicilina. C16H18N2O4S
Partes de una fórmula química
Las fórmulas químicas se componen de símbolos químicos (letras) y subíndices (números), que expresan el tipo de átomos presentes en la sustancia y su cantidad. Sin embargo, en ciertos campos de la química (como la química orgánica) los compuestos muestran cierta recurrencia estructural y funcional, que permite identificar fragmentos de la molécula. Estos fragmentos son llamados “radicales” (unidades moleculares con electrones libres) o “grupos funcionales” (átomos o unidades moleculares responsables de que la sustancia reaccione de una forma determinada).
Ejemplos de grupos funcionales son: hidroxilo (-OH), carbonilo (=C=O), carboxilo (-COOH), entre otros.
Ejemplos de radicales son: metilo (-CH3), etilo (CH3CH2-), entre otros.
Símbolos químicos
Los símbolos químicos son las piezas mínimas que componen a una fórmula química cualquiera y representan a cada uno de los diversos elementos químicos conocidos por la humanidad, o sea, los distintos tipos de átomos de los que está compuesta la materia conocida.
A cada elemento químico le corresponde un símbolo químico particular (generalmente derivado de su nombre histórico en latín).
Algunos ejemplos de símbolos químicos son:
- Carbono. C
- Oxígeno. O
- Fósforo. P
- Hidrógeno. H
- Nitrógeno. N
- Yodo. I
- Hierro. Fe
- Plomo. Pb
- Aluminio. Al
- Selenio. Se
- Plutonio. Pu
Elementos químicos

Los elementos químicos son los diferentes tipos de átomos que componen la materia y que se distinguen entre sí según la configuración particular de sus partículas subatómicas (protones, neutrones y electrones).
Los elementos se pueden agrupar de acuerdo a sus propiedades químicas, o sea, a las fuerzas a las que responden con mayor o menor facilidad, al comportamiento que exhiben en determinadas reacciones, o a otros rasgos propios estructurales.
Un ejemplo que ilustra bien la definición de elemento químico es el siguiente: los isótopos 12C, 13C y 14C son algunos de los isótopos del elemento químico carbono (C).
Los elementos químicos están representados, clasificados y organizados en la Tabla Periódica de los elementos.
Sigue con:
Referencias
- “Fórmulas químicas” https://quimica.laguia2000.com/
- “Significado de las fórmulas químicas” en Gobierno de Aragón. http://aula.educa.aragon.es/
- “Fórmula empírica y molecular” http://bioprofe.com/
- “Chemistry Lesson: Chemical Formulas” (video) en GetChemistryHelp. https://www.youtube.com
- “Chemical Formula” https://www.britannica.com/



¿Te fue útil esta información?
Sí No¡Genial! Gracias por visitarnos :)