Te explicamos qué son los protones, cómo se descubrieron, sus propiedades y características. Además, qué son los nucleones.

¿Qué es un protón?
El protón es un tipo de partícula subatómica, es decir, una de las partículas mínimas que constituyen al átomo. Pertenece a la familia de los fermiones y está dotado de carga eléctrica positiva.
Toda la materia está hecha de átomos, y estos a su vez, están compuestos esencialmente por tres tipos de partículas dotados de carga eléctrica diferente: los electrones (carga negativa), los neutrones (carga neutra) y los protones (carga positiva).
Durante mucho tiempo se pensó que el protón era un tipo fundamental de partícula, es decir, que no se lo podía dividir. Sin embargo, hoy existe sólida evidencia de que está compuesto de quarks.
En todo caso, el protón es una partícula subatómica estable. A diferencia del electrón, que orbita alrededor del núcleo del átomo, los protones se encuentran contenidos en el núcleo atómico junto a los neutrones, aportando la mayor parte de la masa atómica.
Ver también: Modelos atómicos
Descubrimiento del protón

Los protones fueron descubiertos en 1918 por Ernest Rutherford (1871-1937), químico y físico británico. En medio de experimentos con gas de nitrógeno, Rutherford notó que sus instrumentos detectaban la presencia de núcleos de hidrógeno al disparar partículas alfa contra el gas.
Concluyó que estos núcleos debían ser partículas fundamentales de la materia, sin saber en ese entonces que, justamente, el núcleo del átomo de hidrógeno contiene una única partícula: un protón. Fue así que se decidió dotar al hidrógeno del número atómico 1.
Sin embargo, se sabe de experiencias científicas previas que llevaron a este descubrimiento. Por ejemplo, el físico alemán Eugene Goldstein (1850-1930) en 1886 halló iones positivos dentro del átomo, a través de experimentos con rayos catódicos.
Además, el británico J. J. Thompson (1856-1940) ya había descubierto los electrones y su carga negativa, es decir que era necesario que hubiera en el átomo algún otro tipo de partícula con carga opuesta.
Ver además: Modelo atómico de Rutherford
Propiedades y características del protón
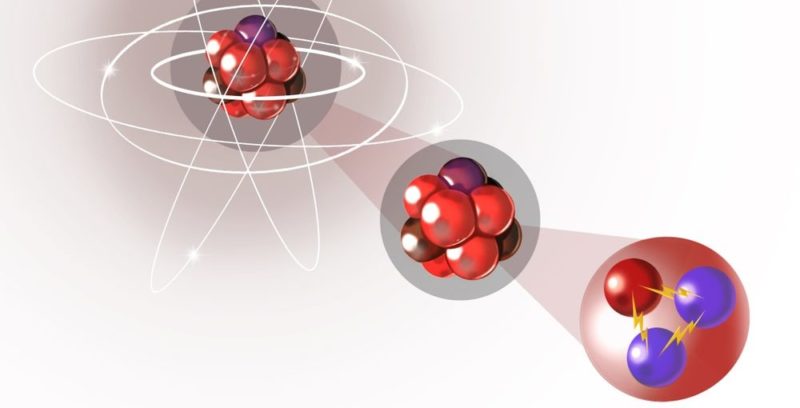
Los protones son partículas compuestas estables, mucho más masivos que un electrón (1836 veces) y dotados de una carga elemental positiva de 1 (1,6 x 10-19 C). Se encuentran compuestos por tres partículas elementales o quarks: dos “up” (arriba) y uno “down” (abajo). Su vida media es superior a 1035 años, momento a partir del cual son susceptibles de descomponerse.
Los protones poseen, como otras partículas subatómicas, un espín propio, o sea, un momento angular intrínseco e invariable, que en este caso es de ½. Esta propiedad resulta particularmente útil para las resonancias magnéticas nucleares y otro tipo de aplicaciones tecnológicas modernas.
Nucleones
Dado que suelen hallarse normalmente en el núcleo atómico, los protones y los neutrones son conocidos como “nucleones”. Los electrones, en cambio, orbitan alrededor de ellos de manera más o menos dispersa.
Los nucleones se hallan unidos entre sí por las fuerzas nucleares fuertes, que solo en casos de átomos particularmente grandes (como el Uranio) pueden ceder ante otras fuerzas, como la electromagnética.
Los nucleones constituyen el mayor porcentaje de la masa de un átomo cualquiera y determinan, por lo tanto, la diferencia entre un elemento químico y el otro: por ejemplo, el átomo de hidrógeno posee únicamente un protón en su núcleo, mientras que el de helio posee dos protones y uno o dos neutrones, dependiendo del isótopo específico.
Número atómico
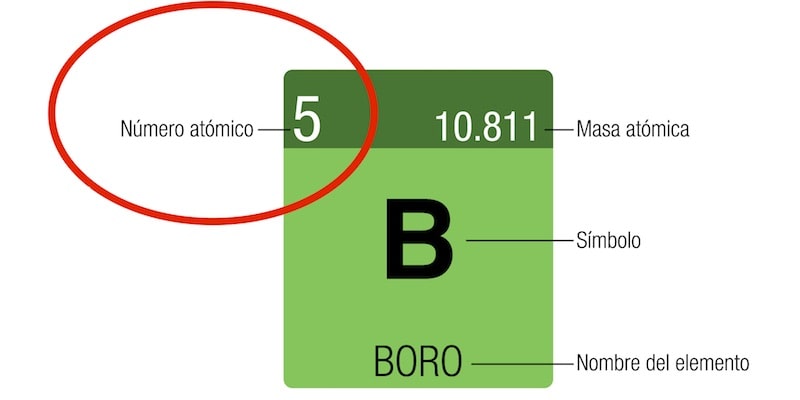
El número atómico (Z) indica cuántos protones posee un tipo de átomo en su núcleo. Cada elemento químico posee un número atómico diferente, aunque su comportamiento químico está más bien determinado por el número de electrones que orbiten en torno a su núcleo (que para un átomo neutro es igual al número de protones).
Así, por ejemplo, el cloro (Cl) posee 17 protones en su núcleo, de modo que su número atómico es 17. Este número no varía nunca, ni siquiera entre los isótopos (versiones) de un mismo átomo, ya que se diferencian entre sí únicamente por el número de neutrones en su núcleo.
Sigue con: Antimateria
Referencias
- “Protón” en Wikipedia.
- “Estructura atómica, átomo, electrón, protón, neutrón, número atómico, de masa, ión” (video) en Academia Internet.
- “El Protón” en Hyperphysics de la Universidad del Estado de Georgia (EEUU).
- “Neutrons and protons in atomic nuclei” en Nature.
- “Proton (subatomic particle)” en The Encyclopaedia Britannica.
¿Te fue útil esta información?
Sí No¡Genial! Gracias por visitarnos :)