Te explicamos qué es un ion y cómo está constituido y algunos ejemplos. Además, qué es un anión y un catión.
¿Qué es un ion?
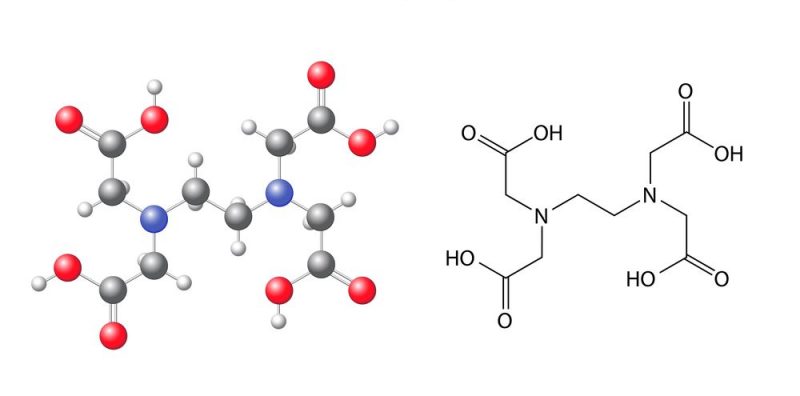
En química, se conoce como ion a una partícula cargada eléctricamente y que está constituida por un átomo o molécula que no es eléctricamente neutro, es decir, que en su constitución ha ganado o perdido electrones. El proceso mediante el cual se producen iones se llama “ionización”.
Los iones pueden estar constituidos por dos o más átomos (poliatómicos) de diversa naturaleza, o de un único átomo (monoatómicos). En cualquiera de los casos, hablaremos de un catión (o cationes) cuando se trate de un ion cargado positivamente (es decir, que el átomo o molécula neutra inicial cedió electrones), y hablaremos de un anión (o aniones) cuando se trate de un ion cargado negativamente (es decir, que el átomo o molécula neutra inicial aceptó electrones).
También se conocen otros tipos de iones, en base a su carga eléctrica, conocidos como dianiones (cuando presentan dos cargas negativas), zwitteriones (cuando presentan una carga positiva y una negativa que están aisladas, pero en el mismo compuesto, debido a lo que es neutro), o radicales iónicos (iones de enorme reactividad e inestabilidad debido a que tienen electrones libres). En líneas generales, los iones son muy reactivos y tienden a combinarse con otros iones, átomos o moléculas por interacciones electrostáticas.
Los iones juegan un papel indispensable en la vida, sobre todo los de calcio, potasio y sodio, cuya importancia en el tránsito de las membranas celulares y en los neurotransmisores se ha estudiado bastante. Por lo demás, la comprensión de los iones nos ha permitido desarrollar la tecnología del plasma e incluso medir la calidad del agua en base a las sales iónicas disueltas en ella.
Ver además: Enlace químico
Anión
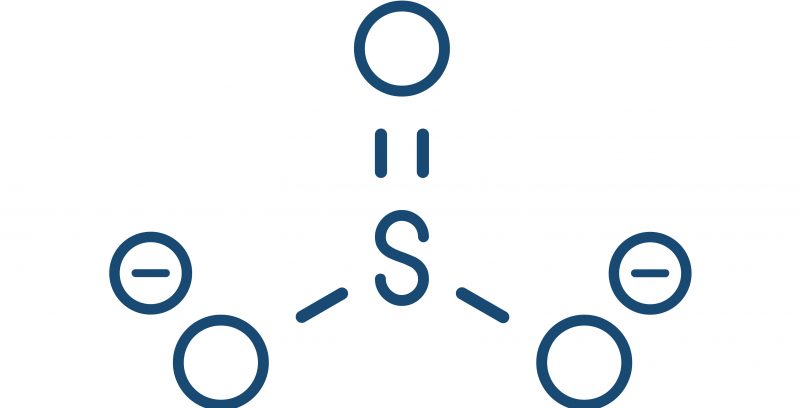
Se conoce como anión (o aniones) a los iones que poseen una carga eléctrica negativa, o sea, que han ganado electrones en una reacción química que les dio origen. Pueden estar constituidos por uno o por varios átomos, pero incluso, en este último caso la carga global de la molécula (su estado de oxidación) es siempre negativa.
Existen tres tipos de aniones:
- Monoatómicos. Aquellos constituidos por un único átomo que ha ganado electrones. Por ejemplo: Cloruro (Cl–).
- Poliatómicos. Provienen de una molécula que ha ganado electrones en una reacción química, o bien de un ácido que ha perdido protones. Por ejemplo: Sulfito (SO32-).
- Ácidos. Provienen de un ácido poliprótico (que poseen múltiples hidrógenos ionizables) al cual se le han extraído protones. Por ejemplo: Fosfato diácido (H2PO4–).
Catión
Los cationes son iones que tienen carga eléctrica positiva, es decir, que han perdido uno o varios electrones. Así, al igual que los aniones, los cationes también pueden estar compuestos por uno o más átomos, siempre que la carga total del compuesto, en este caso, sea positiva.
Una de las funciones más importantes de los cationes es su participación en los procesos biológicos. Por ejemplo, los cationes Na+ y K+ juegan un papel fundamental en la transmisión de impulsos nerviosos.
Ejemplos de ion

Los iones más conocidos son:
- Cationes simples. Compuestos por un sólo átomo con carga positiva:
- Aluminio (Al3+)
- Cesio (Cs+)
- Cromo (III) o ion crómico (Cr3+)
- Cromo (VI) o ion percrómico (Cr6+)
- Hidrógeno o protón (H+)
- Helio o partícula alfa (He2+)
- Litio (Li+)
- Hierro (II) o ion ferroso (Fe2+)
- Hierro (III) o ion férrico (Fe3+)
- Niquel (III) o ion niquélico (Ni3+)
- Estaño (II) o ion estanoso (Sn2+)
- Estaño (IV) o ion estánico (Sn4+)
- Cationes poliatómicos. Compuestos por dos o más átomos con carga positiva:
- Amonio (NH4+)
- Oxonio (H3O+)
- Nitronio (NO2+)
- Mercurio (I) o ion mercurioso (Hg22+)
- Aniones simples. Compuestos por un único átomo con carga negativa:
- Azida (N3–)
- Bromuro (Br–)
- Carburo (C4-)
- Cloruro (Cl–)
- Fluoruro (F–)
- Fosfuro (P3-)
- Nitruro (N3-)
- Sulfuro (S2-)
- Oxoaniones. Compuestos por oxígeno y otros elementos, tienen carga negativa:
- Arseniato (AsO43-)
- Borato (BO33-)
- Hipobromito (BrO–)
- Bicarbonato (HCO3–)
- Clorato (ClO3–)
- Clorito (ClO2–)
- Hipoclorito (ClO–)
- Dicromato (Cr2O72-)
- Hidrógenosulfato o bisulfato (HSO4–)
- Hidrógenosulfito o bisulfito (HSO3–)
- Silicato (SiO44-)
- Aniones de ácidos orgánicos. Provenientes de moléculas orgánicas, tienen carga negativa:
- Acetato (C2H3O2–)
- Oxalato (C2O42-)
- Bioxalato (HC2O4–)
- Otros aniones. Con carga negativa y más de un átomo:
- Bisulfuro (HS–)
- Amiduro (NH2–)
- Cianato (OCN–)
- Tiocianato (SCN–)
- Cianuro (CN–)
- Hidróxido (OH–)
¿Te fue útil esta información?
Sí No¡Genial! Gracias por visitarnos :)