Te explicamos qué es la termodinámica, qué estudia y en qué consiste un sistema termodinámico. Además, cuáles son las leyes de la termodinámica.
¿Qué es la termodinámica?
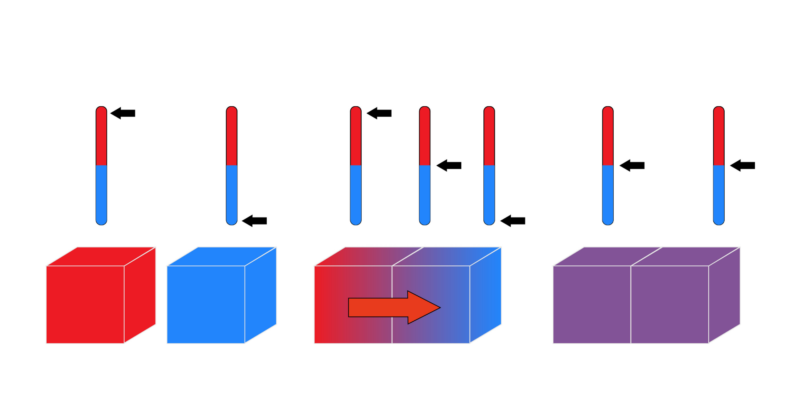
Se llama termodinámica a la rama de la física que estudia las acciones mecánicas del calor y de otras formas semejantes de energía. Su estudio aborda los objetos como sistemas macroscópicos reales, mediante el método científico y razonamientos deductivos, prestando atención a variables extensivas como la entropía, la energía interna o el volumen; así como a variables no extensivas como la temperatura, la presión o el potencial químico, entre otros tipos de magnitudes.
Sin embargo, la termodinámica no ofrece una interpretación de las magnitudes que estudia, y sus objetos de estudio son siempre sistemas en estado de equilibrio, es decir, aquellos cuyas características son determinables por elementos internos y no tanto por fuerzas externas que actúan sobre ellos. Por esa razón, considera que la energía solo puede intercambiarse de un sistema a otro a manera de calor o de trabajo.
El estudio formal de la termodinámica inició gracias a Otto von Guericke en 1650, un físico y jurista alemán que diseñó y construyó la primera bomba de vacío, refutando con sus aplicaciones a Aristóteles y su máxima de que “la naturaleza aborrece el vacío”. Luego de esta invención, los científicos Robert Boyle y Robert Hooke perfeccionaron sus sistemas y observaron la correlación entre presión, temperatura y volumen. Así nacieron los principios de la termodinámica.
La palabra «termodinámica se compone de los vocablos del griego thermós, que significa “calor”, y dynamos, “poder, fuerza”.
Ver además: Calor específico
¿En qué consiste un sistema termodinámico?

Se entiende como sistema termodinámico a una parte del universo que, con fines de estudio, se aísla conceptualmente del resto y se intenta comprender de manera autónoma. Toma nota de los modos en que la energía cambia o se preserva y, al mismo tiempo, de sus intercambios de materia y/o energía con el entorno o con otros sistemas semejantes (de haberlos). Se trata, pues, de un método de estudio de la termodinámica.
El criterio principal de clasificación de estos sistemas se basa en su grado de aislamiento del entorno, distinguiendo así entre:
- Sistemas abiertos. Aquellos que intercambian libremente energía y materia con su entorno, como hacen la mayoría de los sistemas conocidos en la cotidianidad. Por ejemplo: un auto. Uno le entrega combustible y éste devuelve al ambiente gases y calor.
- Sistemas cerrados. Aquellos que intercambian energía con su entorno, pero no materia. Es lo que ocurre con un envase cerrado, como una lata, cuyo contenido es invariable, pero pierde calor con el tiempo, disipándolo en el aire alrededor.
- Sistemas aislados. Aquellos que, hasta cierto punto, no intercambian energía ni materia con el entorno. No existen los sistemas perfectamente aislados, claro está, pero sí hasta cierto grado: un termo que contiene agua caliente preservará su temperatura durante un rato, lo suficiente como para conservarse aislado durante un rato.
¿Cuáles son las leyes de la termodinámica?

La termodinámica se rige por lo establecido en sus cuatro principios o leyes fundamentales, formuladas por diversos científicos a lo largo de la historia de esta disciplina. Dichos principios o leyes son:
- Primer principio, o Ley de la Conservación de la energía. Establece que la cantidad total de energía en cualquier sistema físico aislado de su entorno será siempre la misma, aunque pueda transformarse de una forma de energía a muchas otras diferentes. En menos palabras: “La energía no puede crearse ni destruirse, solo transformarse”.
- Tercer principio, o Ley del cero absoluto. Dicta que la entropía de un sistema que sea llevado al cero absoluto será siempre una constante definida. Esto significa que al llegar al cero absoluto (-273,15° C o 0 K), los procesos de los sistemas físicos se detienen y la entropía posee un valor mínimo constante.
- Principio cero o Ley del equilibrio térmico. Se llama “ley cero” porque, si bien fue la última en postularse, los preceptos básicos y fundamentales que establece tienen prioridad sobre las otras tres leyes. Dicta que “si dos sistemas están en equilibrio térmico de forma independiente con un tercer sistema, deben estar también en equilibrio térmico entre sí”.
Más en: Leyes de la termodinámica
Termodinámica en la química
La termodinámica química es un campo de estudio aparte, centrado en la correlación entre el calor y el trabajo, y las reacciones químicas, todo enmarcado en lo establecido por los principios de la termodinámica. Es decir, se trata de la aplicación de las leyes de la termodinámica, especialmente de las dos primeras, al mundo de las reacciones entre sustancias y compuestos, para obtener así las llamadas “ecuaciones fundamentales de Gibbs”, las cuales rigen el modo en que la energía química contenida en los distintos compuestos cambia y se transmite, o cómo aumenta el grado de entropía del universo cada vez que una reacción espontánea ocurre.
Sigue con:
Referencias
- “Las leyes de la termodinámica en 5 minutos” (video) en Quantum Fracture. https://www.youtube.com/
- “¿Qué es la termodinámica?” https://www.fisicalab.com/
- “Conceptos básicos de termodinámica” en Universidad del País Vasco. http://www.sc.ehu.es/
- “Termodinámica: curso acelerado de física” (video) en Crash Course. https://www.youtube.com/
- “Thermodynamics” https://www.britannica.com/



¿Te fue útil esta información?
Sí No¡Genial! Gracias por visitarnos :)