Te explicamos qué es la evaporación y en qué consiste, con ejemplos. Además, cómo interviene en el ciclo del agua y su diferencia con la ebullición.

¿Qué es la evaporación?
La evaporación es un proceso físico que consiste en la transformación de una sustancia en estado líquido al estado gaseoso. Es un proceso que ocurre en la superficie del líquido, a cualquier temperatura, y de manera lenta y gradual.
Aunque la evaporación de un líquido puede ocurrir a cualquier temperatura, si se aumenta la temperatura del líquido, más rápido ocurre la evaporación.
La evaporación es de vital importancia para sostener la vida en el planeta Tierra, pues es una de las etapas del ciclo del agua, que es un ciclo biogeoquímico mediante el cual el agua se desplaza de una región a otra, garantizando que todos los seres vivos puedan consumirla.
Ver además: Fenómenos físicos
¿En qué consiste el proceso de evaporación?
El proceso de evaporación comienza cuando las moléculas que están ubicadas en la superficie del líquido se mueven en la dirección apropiada y con la energía cinética suficiente para vencer las fuerzas moleculares que las mantienen unidas en la fase líquida.
La energía cinética es la energía que adquiere un cuerpo (en este caso, las moléculas de agua) debido a su movimiento relativo. Cuando aumenta la temperatura, aumenta la energía cinética. Por eso, al aumentar la temperatura del agua, aumenta la energía cinética de sus moléculas y esto hace posible que las moléculas de agua se puedan separar.
Esto ocurre porque una vez que las moléculas que están situadas en la superficie del líquido tienen suficiente energía, vencen las fuerzas de atracción moleculares, se separan y pasan a la fase gaseosa.
Ver también: Cambio físico
Tipos de evaporación
El proceso de evaporación ocurre espontáneamente en la naturaleza al aumentar la temperatura de un líquido, pero también puede ser generado en un laboratorio por la acción del ser humano. En este sentido, se pueden definir dos tipos de evaporación:
- Evaporación natural. Ocurre en la naturaleza, sin la influencia del hombre. Un ejemplo de evaporación natural, es la evaporación del agua de un lago cuando aumenta su temperatura por el calentamiento que provoca el sol.
- Evaporación asistida. Es generada por el ser humano en un laboratorio. Se puede utilizar como un método para separar los componentes de una disolución o de una mezcla.
Ejemplos de evaporación
Algunos ejemplos en los que se puede ver el proceso de evaporación:
- El secado de la ropa mojada puesta al sol, cuando se evapora el agua sobre su superficie.
- El secado natural del cabello húmedo luego de un baño.
- La desaparición paulatina del sudor, luego de hacer ejercicio.
- La evaporación de agua procedente de ríos y mares.
- El secado gradual del suelo luego de haber sido mopeado y fregado con agua.
- La obtención de sal marina a partir de la evaporación del agua de mar en una salina.
- La reducción y desaparición de los charcos que se forman con la lluvia, una vez que esta termina y sale el sol.
- El secado de las gotas de rocío que amanecen sobre las hojas de las plantas a la mañana.
- La evaporación del agua en recipientes de los perros y gatos.
- La evaporación del agua en un jarrón con flores.
Diferencias entre vaporización, evaporación y ebullición

Se denomina vaporización al proceso de cambio de una sustancia del estado líquido al estado gaseoso.
La vaporización puede ocurrir a través de dos procesos:
- La evaporación, que es el paso de una sustancia del estado líquido al estado gaseoso, y ocurre gradualmente en la superficie del líquido y a cualquier temperatura.
- La ebullición, que es el paso de una sustancia del estado líquido al estado gaseoso, y ocurre cuando la temperatura de la masa total del líquido es mayor que su punto de ebullición.
El punto de ebullición de una sustancia líquida es la temperatura a la que su presión de vapor se iguala a la presión la rodea. Si la presión de vapor del líquido es igual a la presión atmosférica (1 atm), entonces se le denomina punto de ebullición normal. El punto de ebullición es específico para cada sustancia.
La evaporación en el ciclo del agua
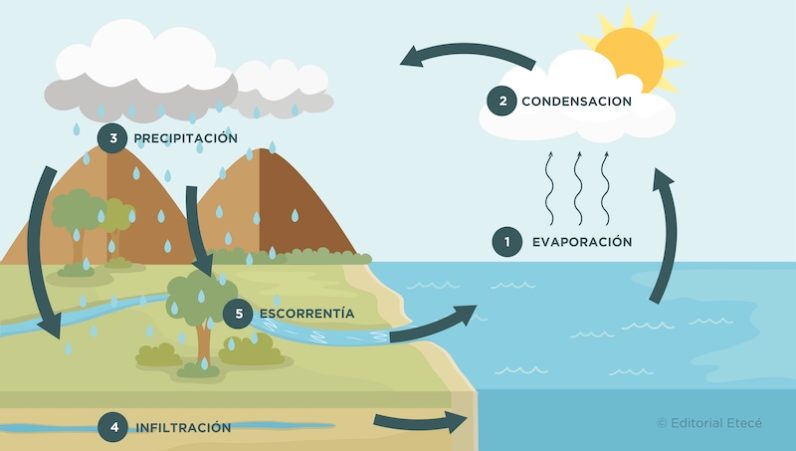
El ciclo del agua o ciclo hidrológico es el proceso mediante el cual el agua circula sobre y por debajo de la superficie sólida de la tierra.
Durante este ciclo el agua se traslada de unas regiones a otras y además, cambia de estado de agregación, es decir, se transforma de líquida a sólida, de sólida a líquida, de líquida a gaseosa, de gaseosa a líquida, de sólida a gaseosa y de gaseosa a sólida.
La evaporación es una de las etapas del ciclo del agua, que comienza cuando el agua que está en la superficie terrestre se evapora. Posteriormente, el vapor de agua asciende (mezclado con el aire) hasta que se enfría, se condensa y forma las nubes (esta etapa se conoce como “condensación”).
Si el clima es cálido, el agua condensada en las nubes cae en forma de gotas hacia la superficie terrestre, lo que se conoce como lluvia o precipitación. Si el clima es frío, el agua puede caer en forma de granizo o nieve.
La evaporación es una etapa muy importante del ciclo del agua, pues garantiza que se mantengan los niveles necesarios de humedad en el aire para mantener la vida en el planeta.
Puede servirte: Ciclo del agua
Evaporación como método de separación de mezclas

El proceso de evaporación se puede utilizar como un método para separar los componentes de mezcla (combinación de dos o más componentes sin implicar uniones químicas entre ellos) o disolución (una mezcla homogénea).
Algunas técnicas para lograr la evaporación de un componente y separarlo del resto son:
Evaporación al aumentar la temperatura de la mezcla
Consiste en calentar una mezcla (generalmente una mezcla sólido-líquido) hasta que las moléculas del líquido adquieran suficiente energía para separarse de la superficie del líquido y pasar a la fase gaseosa. Las moléculas del componente sólido quedan en el recipiente.
Este procedimiento se utiliza para separar mezclas que preferentemente no contengan disolventes inflamables. También se usa para secar sólidos.
Evaporación al disminuir la presión que rodea la mezcla
Consiste en disminuir la presión que rodea una mezcla (mezcla sólido-líquido en este caso), lo que hace que las moléculas del líquido se separen, se liberen (debido a la poca presión sobre ellas) y pasen a la fase gaseosa. Las moléculas del componente sólido quedan en el recipiente.
Este proceso se suele realizar a temperatura ambiente (25 ⁰C ), y se utiliza para secar sustancias que son inestables a altas temperaturas.
Evaporación al combinar el aumento de la temperatura y la disminución de la presión
Consiste en combinar los dos procedimientos anteriores para separar mezclas formadas por componentes con cierta inestabilidad ante temperaturas elevadas.
Un ejemplo de aplicación de la evaporación como un método de separación de mezclas se puede ver en las salinas, que son lugares en los que el sol calienta el agua de mar hasta que el agua pasa al estado gaseoso y la sal sólida queda en el fondo de grandes depósitos.
Más en: Métodos de separación de mezclas
Referencias
- Manzur, A., & Cardoso, J. (2015). Revista mexicana de física E, 61(1), 31-34.
- Fiedler, R. (1955, June). La importancia del proceso de evaporación solar para la industria del Salitre. In Anales del Instituto de Ingenieros de Chile (No. 9-10, pp. ág-397).
- Peter Atkins,Loretta Jones (2012). Principios de química Los caminos del descubrimiento. Editorial Médica Panamericana. ISBN: 09789500602822
¿Te fue útil esta información?
Sí No¡Genial! Gracias por visitarnos :)