Te explicamos qué es el fósforo, y sus principales características. Además, entenderás para qué sirve y dónde se encuentra este elemento químico.
¿Qué es el fósforo?
El fósforo es un elemento químico de la Tabla Periódica que se representa con el símbolo P. Tiene número atómico 15 y masa atómica 30.97 uma. Es un no metal muy reactivo que se encuentra en la corteza terrestre fundamentalmente formando parte de fosfatos inorgánicos (PO43-), que son iones que forman sales. También se encuentra formando parte de los seres vivos.
Además, el fósforo forma varios alótropos, y cada uno tiene distintas propiedades y utilidades en las diversas industrias. Por otra parte, se debe prestar especial atención a los niveles de fósforo en las aguas del planeta, porque cuando se encuentra en niveles excesivos, puede provocar el crecimiento descontrolado de algunas especies acuáticas que afectan al resto de las especies que viven en las aguas.
Puede servirte: Azufre
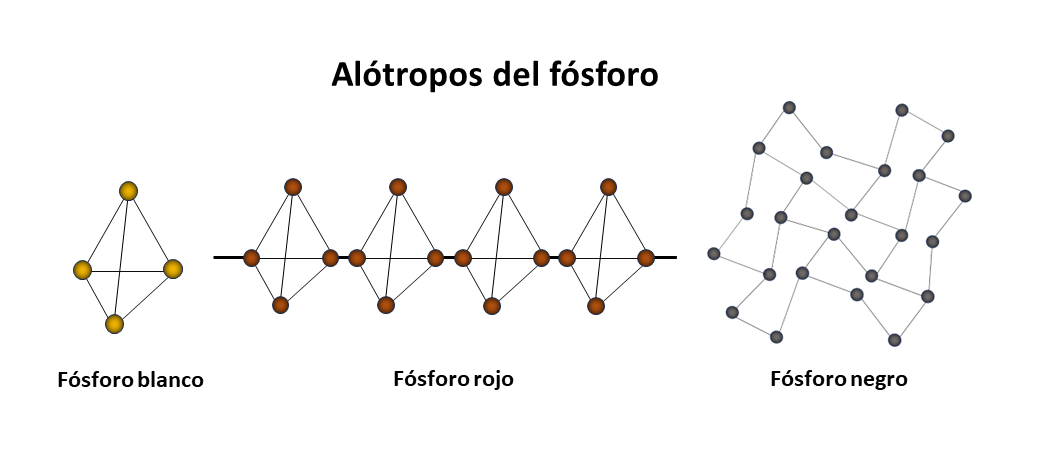
Alótropos del fósforo
Este elemento químico forma varios alótropos. Los alótropos son las distintas formas en que pueden enlazarse los átomos de un elemento químico. Los alótropos del fósforo son el fósforo blanco, el fósforo rojo y el fósforo negro.
- El fósforo blanco es muy tóxico e inflamable.
- El fósforo rojo es más estable y menos tóxico, es el fósforo que se utiliza para fabricar cerillas.
- El fósforo negro no es inflamable y conduce la electricidad.
Algunos ejemplos de las estructuras de los alótropos del fósforo son:
Propiedades del fósforo
El fósforo está presente en compuestos químicos orgánicos e inorgánicos. Por otra parte, el fósforo tiene diferentes propiedades físicas y químicas que varían según el alótropo que está formando. En este sentido, las principales propiedades físicas y químicas del fósforo son:
Propiedades químicas del fósforo
Cuando forma fósforo blanco:
- Es el más reactivo.
- Se oxida espontáneamente con el oxígeno del aire emitiendo luz, lo que se conoce como “fosforescencia”.
- Experimenta una reacción exotérmica (reacción que libera calor) cuando está en contacto con el calor y la luz, y se transforma en fósforo rojo.
Cuando forma fósforo rojo:
- Reacciona de manera violenta con oxidantes para formar pentóxido de fósforo (P2O5). Esta reacción, además, produce un humo blanco.
Propiedades físicas del fósforo
| Propiedad | Fósforo blanco | Fósforo rojo | Fósforo negro |
|---|---|---|---|
| Apariencia | Ceroso, translúcido, blanco a amarillento | Amorfo, rojizo | Similar al grafito, negro |
| Conductividad eléctrica | No conduce la electricidad | No conduce la electricidad | Conduce la electricidad |
| Densidad | Es el más denso | Tiene densidad intermedia | Es el menos denso |
| Toxicidad | Tóxico | Menos tóxico | No tóxico |
| Fenómenos notables | Brilla en la oscuridad (fosforescencia) | Se usa en fósforos de seguridad | Presenta conductividad térmica y eléctrica |
Función biológica del fósforo
El fósforo se considera un elemento químico esencial debido a que forma parte de compuestos químicos que son fundamentales para las funciones vitales de los organismos vivos. Por ejemplo:
- Los fosfatos inorgánicos (PO43-) forman parte de las moléculas de ADN y ARN.
- La molécula de adenosín trifosfato (ATP) es la encargada de transportar y almacenar energía en la célula.
- El fósforo interviene en los procesos de crecimiento, reparación y conservación de tejidos.
- El fósforo forma parte de huesos y dientes.
- El fósforo interviene en el correcto funcionamiento de los riñones, en la contracción muscular y en las señales nerviosas.
¿Para qué sirve el fósforo?

El fósforo se utiliza en diversos procesos llevados a cabo por el ser humano. Se ha utilizado en procesos industriales, en laboratorios y en la medicina. Algunas aplicaciones del fósforo son:
- Se utiliza en la síntesis de diversos compuestos químicos como el tricloruro de fósforo (PCl3) y el pentacloruro de fósforo (PCl5).
- Se utiliza para fabricar las cerillas que mundialmente se han utilizado para generar fuego.
- Puntualmente, el fósforo blanco se ha utilizado para fabricar municiones y generar humo en actividades militares.
- Se emplea para producir abonos.
- Se utiliza en la industria alimenticia para producir aditivos.
- Se usa como componente de productos de limpieza.
¿Dónde se encuentra el fósforo?

El fósforo se encuentra en la naturaleza formando parte de diferentes minerales, como la apatita (Ca5(PO4)3(F,Cl,OH)), que se encuentra principalmente en Rusia, Marruecos y Estados Unidos. Así, el fósforo está presente fundamentalmente formando parte de rocas sedimentarias, que cuando sufren el desgaste debido a las adversidades del clima, liberan el fósforo al suelo y a las aguas. Los sedimentos marinos y los suelos son importantes reservas de fósforo.
Por otro lado, el fósforo forma parte de los seres vivos, pues se encuentra presente en las moléculas de ADN y ARN. Además, semillas, legumbres y verduras también contienen fósforo.
Efectos del fósforo en el medio ambiente
El exceso de fósforo en ríos y lagos produce un proceso llamado “eutrofización”. La eutrofización es el crecimiento excesivo de algas y microorganismos acuáticos por el consumo de altos niveles de nutrientes, como es el caso del fósforo.
Estas algas y microorganismos consumen de manera desmedida el oxígeno disuelto en el agua, lo que provoca la muerte de los seres vivos acuáticos y además, la reducción de las reservas de agua potable.
Así, el fósforo llega a los ríos y lagos como resultado de la escorrentía cuando se vierten excesos de fertilizantes, pesticidas y detergentes. En este sentido, en muchas ocasiones el fósforo ha pasado de ser un nutriente necesario a convertirse en un contaminante.
Por otra parte, el fósforo blanco es muy venenoso e inflamable y, cuando entra en contacto con la piel, produce quemaduras. Además, cuando un ser humano sufre una exposición prolongada al fósforo blanco, sufre fosfonecrosis, que consiste en la necrosis de la mandíbula.
Ciclo del fósforo
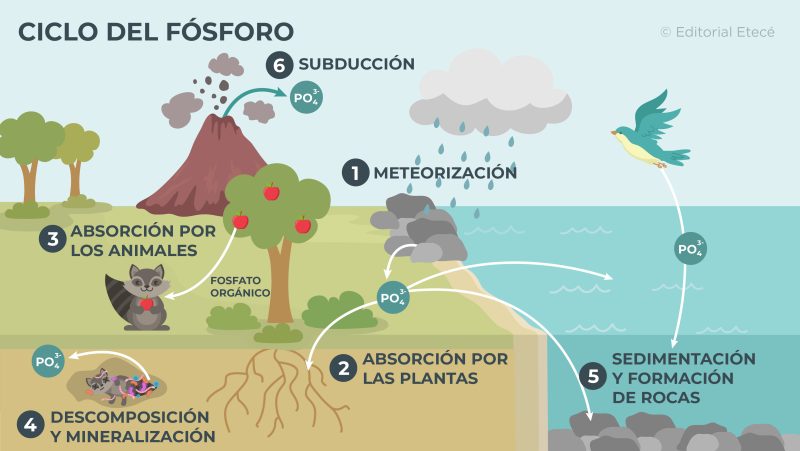
El ciclo del fósforo es la circulación de fósforo en el planeta Tierra. A través de este proceso, el fósforo se traslada entre los distintos ecosistemas y el medio ambiente que los rodea. Es un ciclo bastante lento debido a que el fósforo no forma compuestos químicos volátiles, por lo que no puede pasar a la atmósfera.
El ciclo del fósforo está formado por distintas etapas:
- Meteorización. Consiste en la descomposición de las rocas por impacto del viento, la lluvia, la temperatura y otros agentes erosivos. En el caso de las rocas que contienen fósforo, la meteorización provoca que el fósforo se libere al suelo y a las aguas de mares, ríos y lagos.
- Absorción por las plantas. El fósforo presente en el suelo en forma de fosfatos (PO43-) es absorbido por las plantas a través de sus raíces.
- Absorción por los animales. El fósforo puede ser incorporado a los animales herbívoros cuando consumen plantas y a los carnívoros cuando comen a los animales herbívoros.
- Descomposición y mineralización. El fósforo que contienen las plantas y los animales se libera al suelo cuando estos seres vivos mueren.
- Sedimentación y formación de rocas. El fósforo que se encuentra en el fondo de lagos, ríos y mares es comprimido para formar rocas fosfatadas.
- Subducción. El fósforo presente en las placas hundidas puede regresar hacia la superficie terrestre durante la erupción de los volcanes.
Sigue con:
Referencias
- Fernández, M. T. (2007). Fósforo: amigo o enemigo. ICIDCA. Sobre los Derivados de la Caña de Azúcar, 41(2), 51-57.
- Cerón Rincón, L. E., & Ancízar Aristizábal Gutiérrez, F. (2012). Dinámica del ciclo del nitrógeno y fósforo en suelos. Revista colombiana de Biotecnología, 14(1), 285-295.
- Múnera Vélez, G. A. (2014). El fósforo, elemento indispensable para la vida vegetal. Universidad Tecnológica de Pereira. Book.
- Francis A. Carey, Robert M. Giuliano. (2014) Química Orgánica.McGRAW-HILL/INTERAMERICANA EDITORES, S.A. DE C.V.



¿Te fue útil esta información?
Sí No¡Genial! Gracias por visitarnos :)