Te explicamos qué es el equilibrio térmico, en qué consiste y cuál es su fórmula. Además, la ley cero de la termodinámica y ejemplos.
¿Qué es el equilibrio térmico?
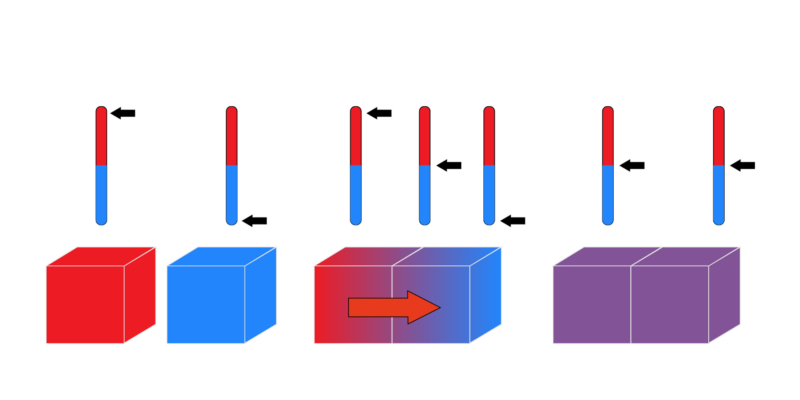
En física, se llama equilibrio térmico al estado en que dos cuerpos en contacto, o separados por una superficie conductora, igualan sus temperaturas inicialmente dispares, debido a la tranferencia de calor de uno hacia el otro.
Si tenemos dos objetos en contacto, uno más caliente que otro, a medida que el tiempo transcurra ambos tenderán a alcanzar la misma temperatura y, si no hay transferencia de calor hacia otros objetos, en adelante mantendrán un equilibrio térmico, o sea, una temperatura constante.
- Ver además: Conductividad térmica
¿En qué consiste el equilibrio térmico?

Este fenómeno puede explicarse microscópicamente, comprendiendo que la temperatura de los objetos está directamente relacionada con la energía cinética promedio de sus partículas, sean átomos, moléculas, o los que convenga considerar. Este promedio es lo que comúnmente se llama en física «energía interna», por lo que a mayor energía cinética mayor energía interna y mayor temperatura del sistema.
Dos cuerpos en contacto intercambian energía a medida que el tiempo transcurre. Y así, el punto de equilibrio térmico se alcanza cuando la energía cinética de ambos cuerpos se iguala, de manera que ambos cuerpos pasan a operar como un sistema termodinámico único, dotado de una misma cantidad de energía interna y, por ende, de temperatura.
Fórmula del equilibrio térmico
La expresión del equilibrio térmico involucra el cálculo de la diferencia de temperaturas entre los dos cuerpos, por lo que debe determinarse la cantidad de calor (Q) que intercambian.
Esto se determina empleando la fórmula Q = m . Ce . Δt, en donde m será la masa del cuerpo, Ce su calor específico expresado en cal / gr °C, y Δt la variación de temperatura, o sea: Δt = tf – ti, temperatura final menos temperatura inicial.
Una vez calculado el calor Q para cada cuerpo, podremos compararlos a sabiendas de que el equilibrio térmico se da en la igualdad de las temperaturas entre el cuerpo 1 y el cuerpo 2. Para llegar al equilibrio térmico, el calor que el cuerpo más frío gana es el que el cuerpo más caliente pierde, así que Q1 = Q2, o sea, calor ganado = calor perdido.
Ley cero de la termodinámica
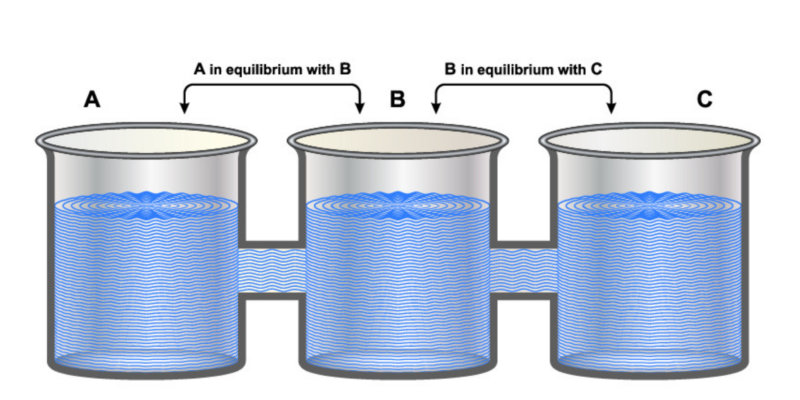
Este principio está expresado en la llamada Ley cero de la termodinámica, que fue expresada en 1931 por R. H. Fowler de la siguiente manera: “Si dos sistemas A y B se encuentran, cada uno por separado, en equilibrio térmico con un tercer sistema, que llamaremos C, entonces A y B se encuentran también en equilibrio térmico entre sí”.
O sea: si A = C y B = C, entonces A = B.
Gracias a este principio, centrado en la formulación matemática de la termodinámica, se sabe lo que Maxwell expresó en palabras de esta manera: “Todo el calor es del mismo tipo”.
Ejemplos de equilibrio térmico
A continuación, algunos ejemplos sencillos de equilibrio térmico:
- Cuando entramos en una habitación caliente, percibimos el calor del aire inmediatamente pero dado un margen de tiempo, nuestro cuerpo intercambiará calor con el aire y entrará en equilibrio térmico con él, así que dejaremos de percibir la diferencia de temperatura.
- Si introducimos un recipiente de vidrio con agua fría dentro de uno mayor con agua hirviendo, el flujo de calor entre ambos enfriará el agua caliente y calentará la fría, hasta alcanzar un nivel de equilibrio térmico intermedio.
- Los productos que tenemos en el congelador de nuestra cocina se hallan en equilibrio térmico respecto del aire helado entre ellos, de modo que todos comparten la misma temperatura.
Sigue con:
Referencias
- “Equilibrio térmico” (video) en Universidad Católica de San Pablo.
- “Thermal equilibirum” en Hyperphysics.phy.
- “The Zeroth Law of Thermodynamics: Thermal Equilibrium” (video) en Dave Explains.
- “Thermal equilibrium” en The Encyclopaedia Britannica.




¿Te fue útil esta información?
Sí No¡Genial! Gracias por visitarnos :)